Máquina de blísteres para Pequeñas empresas farmacéuticas y fabricantes por contrato: La guía definitiva del comprador
Seleccionar el máquina de blíster para farmacias pequeñas no sólo le cuesta capital, sino también preparación para auditorías, velocidad de cambio de formato y, en última instancia, los contratos que financian su crecimiento. Esta guía, de eficacia probada en la práctica, le ayudará a acertar a la primera.
Según Forester Xiang, fundador de HIJ Machinery con 20 años de experiencia en plantas de producción desde Bogotá a Bangkok: Las OCM que adquieren envasadoras blíster sin documentación IQ/OQ se enfrentan a costes de recalificación que multiplican por 3 su inversión en equipos originales. cuando se auditen conforme a FDA 21 CFR Parte 211 o EU GMP Anexo 1 (revisión 2022).
👤 La visión del guardabosque
Perspectiva de 20 años sobre el terrenoLa respuesta directa: Para los pequeños fabricantes farmacéuticos y por contrato, la máquina de envasado en blíster adecuada no es la más barata, sino la que se adapta a su cartera de contratos sin provocar un costoso restablecimiento de la conformidad cada vez que cambie su SKU.
La experiencia de campo y la trampa oculta: En los 20 años que llevo recorriendo plantas de producción desde Bogotá hasta Bangkok, he visto cómo innumerables OCM compraban blísteres independientes de bajo coste sin ninguna documentación de GMPc, para meses más tarde suspender las auditorías de la FDA o del Anexo 1 de la UE, absorbiendo unos costes de recalificación que triplicaban su inversión original. La trampa oculta de la que nadie te advierte: las máquinas económicas rara vez se entregan con protocolos IQ/OQ o con soporte FAT/SAT adecuado, dejando que su equipo escriba documentos de validación fantasma bajo presión reguladora.
El asesoramiento estratégico: Antes de firmar cualquier pedido, exija una revisión completa del URS y confirme que el proveedor puede validar el cambio de formato en varios tipos de productos, no sólo en la tableta de demostración. En HIJ, nuestra filosofía de integración llave en mano significa que los compradores de pequeña y mediana escala obtienen la misma columna vertebral de ingeniería alineada con cGMP que los grandes fabricantes, sin el precio empresarial. Compre conformidad una vez; escale con confianza.
Lo ideal máquina de blíster para el envasado de blísteres de pequeñas farmacias y farmacias por contrato es un termoformadora o envasadora de blísteres de alu-alu con una capacidad de 30-120 blísteres/min., Se suministra con documentación IQ/OQ/PQ completa, conjuntos de herramientas multiformato y un registro de auditoría basado en PLC que cumple la norma 21 CFR Parte 11. La documentación de conformidad no es negociable: los equipos que no la tengan no pasarán la inspección FDA o EU GMP Anexo 1 (2022), generando costes de revalidación que habitualmente superan los $80.000 USD por ciclo de auditoría.

HIJ DPP-250 Máquina termoformadora de blísteres farmacéuticos - punto de entrada ideal para pequeñas operaciones farmacéuticas que requieren cumplimiento de cGMP y flexibilidad de formato multi-SKU.
Por qué la selección de la blisteadora es una decisión de cumplimiento -no sólo una decisión de inversión- para las pequeñas farmacéuticas y las OGC
Una línea de envasado en blíster para farmacia por contrato debe hacer dos cosas simultáneamente: producir con una economía unitaria viable y satisfacer la inspección reglamentaria que sigue a cada nuevo contrato de cliente. Los pequeños operadores farmacéuticos y las OCM, que suelen fabricar entre 2 y 8 referencias con demandas de producción de entre 30.000 y 500.000 blísteres al día, se enfrentan a un cálculo de selección fundamentalmente diferente al de los fabricantes de gran volumen que fabrican un solo producto 24 horas al día, 7 días a la semana.
La principal realidad operativa: la máquina de blíster de una OCM debe completar cambios de formato validados en menos de 30 minutos para seguir siendo rentable cuando se cambia entre productos de clientes. Cada conjunto de herramientas (molde de formación, matriz de sellado, matriz de punzonado) debe estar documentado, controlado por versiones y ser trazable según los requisitos de recalificación del Anexo 3 del TRS 992 de la OMS y el Anexo 15 del GMP de la UE. Una máquina que logra 200 blísteres/min pero requiere 4 horas de cambio no validado es un pasivo, no un activo.
Tres configuraciones de máquinas dominan el segmento de las pequeñas farmacéuticas y las OCM. Cada una de ellas conlleva distintas implicaciones de cumplimiento:
Empaquetadora semiautomática de blísterRendimiento: 15-40 blísteres/min. Coste inicial más bajo ($8.000-$28.000 USD). Capacidad de auditoría limitada. Adecuada para OGC en fase de I+D con <50.000 unidades/día. Normalmente requiere documentación de validación complementaria.
Termoformado automático (PVC/PVDC)Producción: 40-200 blísters/min. Coste medio ($25.000-$90.000 USD). Registro de auditoría PLC completo. La plataforma estándar del sector para comprimidos, cápsulas y píldoras. Perfil de cambio de formato más flexible.
Ampolla de Alu-Alu conformada en fríoRendimiento: 30-120 blísteres/min. Coste unitario más elevado ($55.000-$150.000+ USD). Obligatorio para API sensibles a la humedad que requieren una barrera MVTR de 0,01-0,1 g/m²-día. Exigido por el Anexo 1 de BPF de la UE para varias categorías de sustancias controladas.
El reto de la CMO multi-SKU: por qué la validación del cambio de formato es su especificación #1
Valide la máquina una vez para el producto A. Ahora su nuevo cliente le pide el producto B con un diámetro de comprimido diferente (12 mm frente a 9 mm), un formato de blíster distinto (4×7 frente a 3×5) y un recubrimiento de PVDC en lugar de papel de aluminio. Sin una máquina diseñada para un cambio rápido y documentado, se enfrenta a un ciclo completo de recalificación según el Anexo 15 de GMP de la UE, que cuesta entre 3 y 6 semanas y entre $15.000 y $40.000 por cambio, dependiendo de su mercado regulador. Las series DPP-250 y DPP-260 de HIJ están diseñadas con mecanismos de bloqueo de utillaje que permiten documentar el cambio de formato en menos de 2 horas, utilizando conjuntos de utillaje numerados que se asignan directamente a su registro de desviaciones URS.

Las operaciones de envasado en blíster que cumplen las cGMP requieren tanto la capacidad de registro de auditoría del lado de la máquina como protocolos de documentación del operario; ambos deben especificarse en su URS.
Modos de fallo comunes y solución de Forester - Fase de selección de la máquina
- 🔴 Síntoma: Una OCM adquiere una envasadora de blíster de bajo coste; 8 meses después, no supera la auditoría del anexo 1 de BPF de la UE debido a la ausencia de registro de temperatura de sellado y de documentación sobre la calidad de los productos.
⚙️ Causa raíz: El PLC de la máquina utiliza un formato de datos patentado, no exportable, sin pista de auditoría conforme a 21 CFR Parte 11. El controlador de temperatura de la mordaza de sellado carece de trazabilidad de calibración (deriva de tolerancia >±5 °C no detectada).
🔧 Arreglo de Forester: Especifique como mínimo un PLC Siemens S7-1200 o Allen-Bradley ControlLogix con registros de lotes exportables CSV. La tolerancia de temperatura de la mordaza de sellado debe ser ≤±2°C con registro del ciclo de calibración de 4 horas. Confirme la disponibilidad de la plantilla IQ/OQ antes de firmar el pedido. - 🔴 Síntoma: El cambio de formato de blíster de 10×1 comprimidos a blíster de 5×2 cápsulas lleva más de 6 horas; la OCM pierde $12.000 en tiempo de producción por cambio.
⚙️ Causa raíz: Los conjuntos de herramientas no están numerados ni controlados por versiones; la alineación de los moldes de conformado requiere un calce manual sin puntos de referencia de repetibilidad.
🔧 Arreglo de Forester: Se requieren máquinas con portaherramientas indexados (alineación de pasadores) y números de serie de herramientas grabados con láser que se correspondan con el catálogo de piezas de cambio validado. Tiempo de cambio objetivo: <45 minutos desde el último blíster en buen estado hasta el primer blíster en buen estado del nuevo formato, totalmente documentado. - 🔴 Síntoma: Fallos en la integridad del sellado a un ritmo de 15-18% en centros de producción con clima húmedo (Sudeste Asiático, Latinoamérica), que han provocado la retirada de productos.
⚙️ Causa raíz: La distribución del calor de la estación de sellado no es uniforme en toda la anchura de la mordaza (diferencia de >8°C del centro al borde); el control inadecuado de la tensión de la lámina provoca microarrugas en el film de tapa.
🔧 Arreglo de Forester: Especifique el control de temperatura de sellado multizona con uniformidad de ≤3°C entre mordazas. El servocontrol de la tensión de la lámina (0,5-5,0 N ajustable) evita que la tapa se arrugue. Validación según ASTM F2338 (pruebas no destructivas de integridad del envase) con registros de pruebas de descomposición al vacío 100%.
Especificaciones técnicas fundamentales para las máquinas de envasado blíster de farmacia por contrato: Qué debe cubrir su URS
Especificar una envasadora de blíster sin una Especificación de Requisitos del Usuario (URS) es el camino más rápido hacia un ciclo de Cualificación (IQ/OQ/PQ) fallido. La URS vincula sus obligaciones normativas con las capacidades técnicas de la máquina y, en el caso de las OGC, debe tener en cuenta su cartera de productos más amplia posible, no sólo su lista de clientes actual. Los 9 parámetros técnicos siguientes representan la especificación mínima viable para cualquier máquina de blíster de calidad farmacéutica destinada a mercados regulados por la FDA o las GMP de la UE.
Termoformado vs. Conformado en frío de Alu-Alu: Elección de la plataforma adecuada para su cartera de API
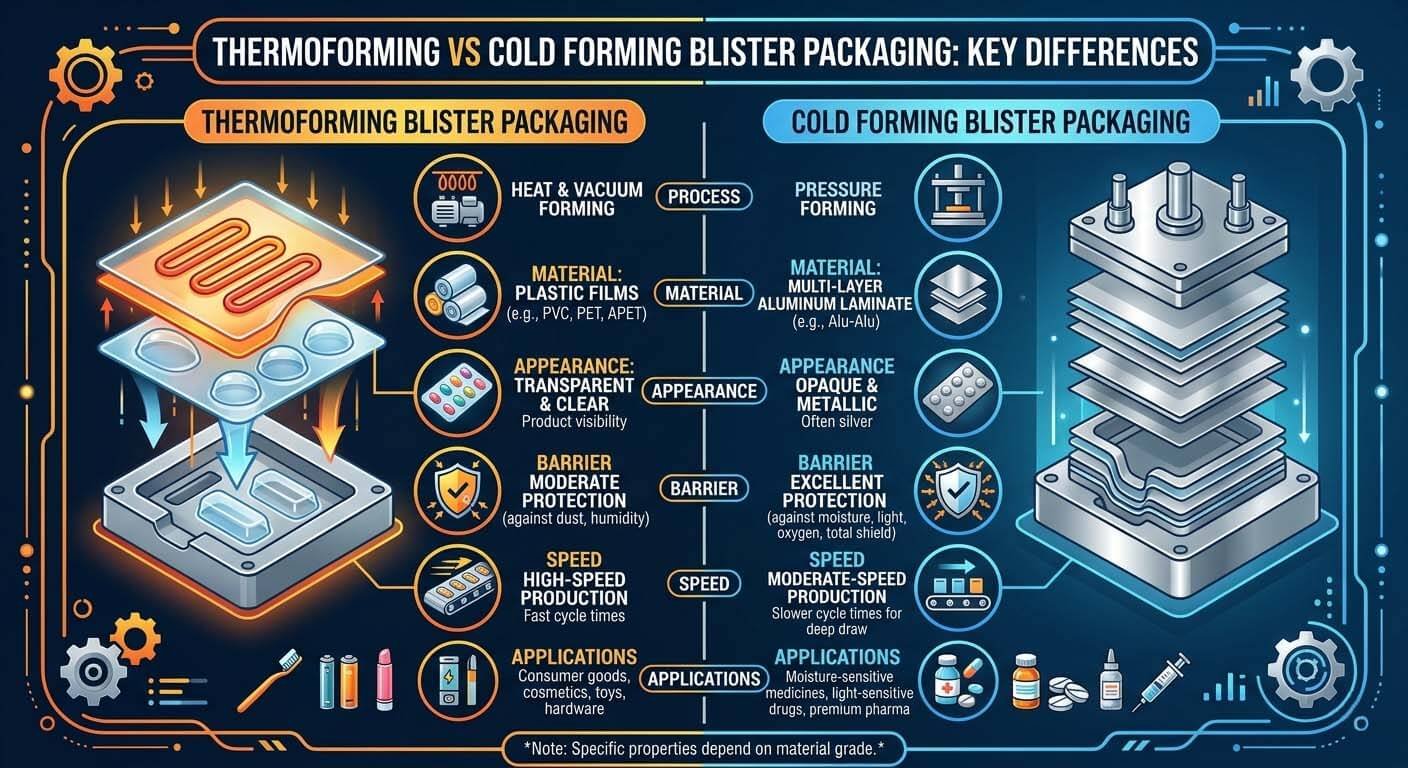
Termoformado (PVC/PVDC) frente a Alu-Alu conformado en frío: la diferencia de rendimiento de barrera determina qué plataforma exige su cartera de API.
| Parámetro | HIJ Termoformado (DPP-250/260) | HIJ Alu-Alu conformado en frío (DPH-300) | Máquinas presupuestarias genéricas |
|---|---|---|---|
| Velocidad de salida | 40-200 ampollas/min | 30-120 ampollas/min | 20-80 ampollas/min |
| Formación de la película | PVC, PVDC, PVC/PE, PP | Alu/PVC/PE (lámina conformada en frío) | Sólo PVC (la mayoría de los modelos) |
| Barrera contra la humedad (MVTR) | 0,3-3,0 g/m²-día (PVDC) | <0,01 g/m²-día (superior) | No especificado / sin clasificar |
| Control de la temperatura de sellado | Multizona ±2°C | Multizona ±2°C | Zona única ±8-15°C |
| PLC / Registro de auditoría | Siemens S7 / Allen-Bradley; preparado para 21 CFR Pt 11 | Siemens S7 / Allen-Bradley; preparado para 21 CFR Pt 11 | Propietario; sin función de exportación |
| Documentos IQ/OQ/PQ | Plantillas completas FAT/SAT + IQ/OQ/PQ | Plantillas completas FAT/SAT + IQ/OQ/PQ | Ninguno de serie; presupuesto aparte |
| Cambio de formato | <45 min con herramientas indexadas | <60 min con herramientas indexadas | 3-8 horas; sin repetibilidad |
| CE / OMS GMP | Certificado CE; alineado con las GMP de la OMS | Certificado CE; alineado con las GMP de la OMS | CE solicitada; sin documentación |
| Prueba de integridad del sellado | Compatible con ASTM F2338 / USP . | Compatible con ASTM F2338 / USP . | Sólo visual; sin datos instrumentales |
| Gama de precios (USD) | $28,000–$75,000 | $55,000–$130,000 | $6,000–$22,000 |
Explora toda la Línea de productos de la máquina de envasado en blíster HIJ incluidas las variantes de termoformado, alu-alu, blíster para líquidos y blíster para cápsulas, todas ellas diseñadas conforme a las normas cGMP.
Los 9 parámetros URS no negociables para los equipos de envasado en blíster de OCM
- Uniformidad de temperatura de la mordaza de sellado ≤±2°C - Una desviación de 12°C en la temperatura de la mordaza provoca una caída de 40% en la integridad del sellado a lo ancho del blíster, según los datos de validación ASTM F2338. El control PID multizona es obligatorio.
- Registros electrónicos de lotes conformes con 21 CFR Parte 11 - Requiere registros de datos con sello de fecha y hora, atribuidos al operador y a prueba de manipulaciones para cada ejecución de producción. Exportación obligatoria a CSV o SQL para la presentación reglamentaria.
- Tiempo de cambio validado ≤60 minutos para todas las combinaciones de formatos documentadas en su catálogo de productos - medido desde el último blíster en buen estado (Formato A) hasta el primer blíster en buen estado (Formato B), totalmente trazable.
- Especificación MVTR para película conformada - Mínimo: PVC ≤3,0 g/m²-día; PVDC ≤0,3 g/m²-día; alu-alu ≤0,01 g/m²-día. Debe acreditarse mediante certificado de análisis del proveedor de la película en DHF.
- Sistema de rechazo con inspección de cavidades 100% - Detección de cavidad vacía mediante cámara o peso con rechazo automático; los eventos de rechazo se registran en el registro de lotes según 21 CFR Parte 211 Subparte K.
- Superficies de contacto de acero inoxidable de calidad GMP - SS 316L para todas las piezas en contacto con el producto; acabado superficial Ra ≤0,8 μm; soldaduras sin grietas según la norma ASME BPE.
- Protocolo FAT (prueba de aceptación en fábrica) - Funcionamiento comprobado durante un mínimo de 4 horas a la velocidad especificada con un índice de defectos <0,5%; todas las funciones de alarma y enclavamiento de seguridad comprobadas y documentadas.
- Paquete de plantillas IQ/OQ/PQ - Plantillas maestras proporcionadas por el proveedor que se ajusten a los requisitos de los sistemas de calidad farmacéutica del anexo 15 de las prácticas correctas de fabricación de la UE y de la norma ICH Q10. Las plantillas deben ser editables y personalizables.
- Garantía de disponibilidad de piezas de repuesto: 10 años como mínimo - Confirmado por escrito, incluidas las piezas de desgaste críticas: molde de conformación, matriz de sellado, herramienta de punzonado, junta de sellado, seguidor de leva.
Anexo 15 de las PCF de la UE
21 CFR Parte 211
21 CFR Parte 11
OMS TRS 992 Anexo 3
ICH Q10
ASTM F2338
USP
ISO 13849-1
Modos de fallo comunes y solución de Forester - Fase de especificación técnica
- 🔴 Síntoma: El sello del blíster no pasa la prueba de descomposición al vacío (USP Método B) con una tasa de defectos de 8% después de 3 meses de funcionamiento - el auditor lo marca como desviación crítica según 21 CFR Parte 211.134.
⚙️ Causa raíz: La dureza de la junta de sellado ha pasado de Shore A 55 a Shore A 72 debido a los ciclos térmicos; combinado con la inconsistencia de la tensión de la lámina de tapa (±18% medido), causando defectos de sellado de microcanales invisibles a la inspección visual.
🔧 Arreglo de Forester: Aplicar un programa PM de 500 horas para la sustitución de la junta de estanqueidad. Especificar que el material de la junta sea silicona (grado HTV, Shore A 50-60 a temperatura de funcionamiento). Instalar una célula de carga de tensión de lámina (objetivo: 2,5 N ± 0,3 N) con registro de lotes en tiempo real. Recalificar según USP Método B después de cada cambio de junta. - 🔴 Síntoma: Los comprimidos se fracturaron en 3-5% de blísteres durante el formado a alta velocidad a 160 blísteres/min; la reclamación del cliente desencadena la observación 483 de la FDA.
⚙️ Causa raíz: La temperatura de la placa calefactora fijada a 180°C en una película de PVC para 155-165°C; la película demasiado blanda se colapsa parcialmente bajo el peso de la tableta durante la transferencia de la cavidad, causando fracturas por impacto en el borde de la tableta.
🔧 Arreglo de Forester: Recalibrar la estación de formado a 158°C ± 2°C para película de PVC de 250 μm. Verificar con termómetro IR en todo el ancho de formado (9 puntos de medición). Habilite el rechazo de recuento de comprimidos para blísteres parciales; registre todos los eventos de rechazo según 21 CFR Parte 211. - 🔴 Síntoma: Los registros de lotes PLC no pueden exportarse ni imprimirse en formato auditable - Un inspector de la FDA emite una observación 483 por incumplimiento del 21 CFR Parte 11.
⚙️ Causa raíz: La máquina se entrega con una HMI de pantalla táctil patentada que almacena los datos en formato binario; sin exportación USB ni conectividad de red; sin control de acceso basado en funciones ni capacidad de firma electrónica.
🔧 Arreglo de Forester: Especifique PLC Siemens S7-1500 o Allen-Bradley ControlLogix con interfaz WinCC SCADA. Requisitos: (1) inicio de sesión basado en funciones con un mínimo de 3 niveles de acceso, (2) exportación a CSV con sello de fecha y hora y suma de comprobación digital, (3) retención local de datos de 30 días como mínimo, (4) documento matriz de conformidad con 21 CFR Parte 11 proporcionado por el proveedor antes del pedido.
Validación IQ/OQ/PQ para líneas de envasado blíster de OCM: Qué debe ofrecer su proveedor
La validación es el proceso mediante el cual su equipo -y su autoridad reguladora- confirman que una máquina de blíster produce de forma constante productos que cumplen las especificaciones de calidad predeterminadas. Para las OGC que trabajan con contratos de envasado farmacéutico en blíster, la carga de la validación se amplifica: cada nuevo producto del cliente suele desencadenar un evento de recalificación, y una máquina que no se diseñó para un cambio documentado generará unos costes de validación que destruirán el margen de su proyecto en 18 meses.
La secuencia DQ → IQ → OQ → PQ no es una sobrecarga burocrática: es su escudo de responsabilidad. Según el anexo 15 (2015) de las BPF de la UE y la subparte J de la parte 21 del CFR, un registro de IQ (Cualificación de la instalación) incompleto o inexistente hace que todos los lotes posteriores fabricados en ese equipo sean potencialmente no reutilizables. Esto es lo que cada etapa debe documentar para una línea de envasado en blíster:

El ciclo de vida de validación DQ → IQ → OQ → PQ: toda máquina de envasado en blíster que entre en una instalación regulada de OCM debe completar esta secuencia antes de la liberación de lotes comerciales.
La hoja de ruta de validación DQ → IQ → OQ → PQ para equipos de envasado en blíster.
-
DQ - Cualificación del diseño: Bloquee su URS antes de realizar el pedidoDocumente que el diseño de la máquina cumple sus requisitos normativos y operativos antes de la compra. Entregables de la DQ: URS completa, lista de comprobación de la DQ del proveedor firmada por una persona cualificada, evaluación de riesgos según ICH Q9 que cubra la integridad del sellado, los materiales en contacto con el producto y la integridad de los datos. Confirme aquí la decisión sobre la plataforma de alu-alu frente a la de termoformado: el cambio de plataforma después de la DQ provoca una revalidación completa.
-
FAT - Prueba de aceptación en fábrica: Calificación en la planta del proveedorRealización de una prueba de producción de 4 horas como mínimo en las instalaciones del proveedor a la velocidad de producción especificada. La lista de comprobación FAT debe incluir: todas las pruebas de alarma (película baja, blíster desalineado, desviación de temperatura >5°C), extracción de muestras de integridad de sellado (mínimo 30 blísteres por formato), demostración de cambio para cada conjunto de herramientas de su catálogo de productos y verificación de exportación de datos. HIJ incluye plantillas de protocolo FAT de serie; exija el informe FAT firmado como condición previa para el pago final.
-
IQ - Cualificación de la instalación: Documentar lo que llegó y cómo se instalóVerificar que la máquina instalada se ajusta a las especificaciones de diseño aprobadas. La lista de comprobación de IQ incluye: referencia cruzada del número de serie del equipo con el pedido, verificación de la conexión de servicios (aire comprimido: 6-8 bar ±5%; electricidad: 380V/50Hz ±3%), confirmación del acabado superficial GMP (SS316L, Ra ≤0,8 μm), certificados de calibración de todos los instrumentos (termopar, manómetro, célula de carga), bloqueo de la versión de software con suma de comprobación y registro de la instalación conforme a obra. IQ debe ser revisado y firmado por la persona de control de calidad de su sitio y el ingeniero de instalación del proveedor.
-
OQ - Cualificación operativa: Probar cada función al límiteDemostrar que la máquina funciona dentro de las especificaciones en todo su rango de funcionamiento, no sólo en el punto de ajuste nominal. La calidad operativa de las envasadoras de blíster debe incluir: prueba de temperatura de sellado a ±5 °C del punto de ajuste nominal (confirmar que se mantiene la integridad del sellado en ambos extremos), prueba de rango de velocidad de 20% a 100% de salida nominal, prueba de precisión de rechazo de cavidades vacías (inyectar 50 cavidades vacías intencionadamente; confirmar el índice de rechazo de 100%), prueba funcional de alarmas y enclavamientos para todas las alarmas enumeradas en 12-20, y un funcionamiento continuo de 4 horas a velocidad nominal con OEE ≥92%.
-
PQ - Cualificación del rendimiento: Tres lotes validados consecutivosProducir 3 lotes consecutivos a escala comercial de su primer producto registrado, cumpliendo cada uno de ellos todos los criterios de aceptación predeterminados. Los criterios de aceptación PQ deben incluir: integridad del sellado según USP Método B (objetivo de defecto 0%; máximo 0,1% AQL), uniformidad de peso dentro de ±3% del peso nominal del comprimido por cavidad, integridad del registro de lotes (100% campos rellenados, sin correcciones manuales sin registro de desviación firmado) y rendimiento de cambio para cada formato adicional de su catálogo de productos validado.
-
En curso: Recalificación anual y control de cambiosCualquier cambio en el proveedor del film de conformado, la especificación de la lámina de sellado, el conjunto de herramientas, la versión del software PLC o el material de la junta de sellado desencadena una revisión del control de cambios en virtud de la Sección 13 del Anexo 15 de BPF de la UE. Clasifique cada cambio como menor (sólo notificación), moderado (recalificación parcial de las funciones afectadas) o mayor (repetición completa de OQ/PQ). Inclúyalo en su programa de mantenimiento preventivo a intervalos de 12 meses, como mínimo.
Para los CMO que estén considerando una línea blíster-a-cartón totalmente integrada con una única columna vertebral de validación, explore Soluciones de envasado llave en mano de HIJ - diseñado para minimizar la carga total de trabajo de validación en todo el conjunto de envasado secundario.
Modos habituales de fallo y solución de Forester - Fase de ejecución de la validación
- 🔴 Síntoma: La OQ falla en la prueba de rechazo de cavidades vacías: 4 de 50 blísteres vacíos intencionadamente pasan sin ser detectados, lo que provoca una desviación crítica de la OQ que detiene la validación durante 6 semanas.
⚙️ Causa raíz: Umbral de sensibilidad del sistema de inspección por cámara fijado de forma demasiado amplia (el área de detección sólo cubre 60% de la profundidad de la cavidad); una cavidad medio llena con un fragmento de comprimido fracturado pasa el umbral.
🔧 Arreglo de Forester: Reconfigure la zona de detección del sistema de visión para cubrir 95% del volumen de la cavidad (ajuste la máscara ROI en HMI). Ajuste el umbral de rechazo de reserva basado en el peso a ≥±15% del peso nominal del comprimido. Vuelva a ejecutar la prueba de inyección de 50 cavidades; documente como desviación OQ con CAPA. Objetivo: 0/50 escapes antes de recalificar. - 🔴 Síntoma: El lote 2 de PQ no supera la comprobación de integridad del registro de lotes: se han encontrado 12 entradas manuales sin registro de desviaciones, lo que se considera una posible violación de la integridad de los datos según los principios ALCOA+.
⚙️ Causa raíz: Deficiencia en la formación de los operarios: el personal no es consciente de que cualquier anulación manual del valor de consigna del PLC debe registrarse como un evento de desviación, y no sólo anotarse en el libro de registro.
🔧 Arreglo de Forester: Implantar un bloqueo de la HMI basado en funciones que obligue a rellenar un formulario de entrada de desviaciones cada vez que se ajuste manualmente un valor de consigna fuera de ±5% del rango validado. Formar a todos los operarios en los requisitos ALCOA+ (Atribuible, Legible, Contemporáneo, Original, Exacto + Completo, Coherente, Duradero). Emitir CAPA; reejecutar PQ Lote 2 después de 30 días de confirmación de cierre de CAPA.
Proceso de compra paso a paso: Cómo deben evaluar y adquirir una máquina de envasado en blíster las pequeñas empresas farmacéuticas y las OCM
Las decisiones de compra de equipos de envasado en blíster son irreversibles durante 10-15 años. Un proceso de aprovisionamiento estructurado elimina los tres errores de compra más comunes: comprar para la capacidad de hoy en lugar de para la cartera de contratos de mañana, no especificar suficientemente los requisitos de documentación de conformidad y seleccionar proveedores que desaparecen después de la puesta en servicio. Este marco de 7 pasos se deriva de la experiencia directa de Forester en la calificación de proveedores para clientes de OCM en el sudeste asiático, América Latina y Oriente Medio.
-
Mapee toda su cartera de productos, no sólo las referencias actualesHaga una lista de todos los tipos de producto que su acuerdo con la OCM podría exigirle envasar en los próximos 5 años: tamaños de comprimidos (6-22 mm), tamaños de cápsulas (00-5), formatos de blíster, tipos de película (PVC, PVDC, alu-alu) y mercados reguladores (FDA, UE, OMS). Esto define su catálogo de herramientas y determina si el termoformado o el conformado en frío es su plataforma de referencia. Una máquina especificada sólo para su cliente actual se convertirá en su futuro cuello de botella.
-
Redacte su URS antes de ponerse en contacto con cualquier proveedorUn proveedor que recibe una URS y responde con objeciones o solicitudes de revisión le está diciendo algo importante sobre su capacidad de ingeniería. Su URS debe especificar: el rango de velocidad de salida, la compatibilidad de la película de conformado, la tolerancia de control de la temperatura de sellado, la marca del PLC y el estado de cumplimiento del 21 CFR Parte 11, el paquete de documentos de validación, el objetivo de tiempo de cambio por par de formato y los requisitos de asistencia posventa, incluido el SLA de tiempo de respuesta y la duración de la garantía de piezas de repuesto.
-
Preselección de proveedores basada en pruebas de cumplimiento, no en folletosSolicite lo siguiente a cada uno de los proveedores preseleccionados: (1) modelo de plantilla IQ/OQ/PQ para su modelo de máquina, (2) lista de referencia de más de 3 clientes CMO o farmacéuticos en su mercado regulatorio con permiso de contacto, (3) certificado CE con número de organismo notificado, (4) documento de procedimiento FAT que muestre los parámetros de prueba y los criterios de aceptación, (5) matriz de cumplimiento 21 CFR Parte 11. Los proveedores que no puedan proporcionar los puntos 1, 3 y 4 deben ser eliminados independientemente del precio.
-
Realice una auditoría de fábrica - o exija una FAT de vídeo en directoPara inversiones superiores a $30.000 USD, la auditoría de fábrica no es opcional. Confirme: Entorno de fabricación conforme a las GMP (zona de montaje cerrada, humedad controlada), capacidad de calibración interna de los instrumentos de temperatura y presión, máquina real funcionando a la potencia especificada con las dimensiones de la pastilla/cápsula de su producto (traiga muestras) y sistema de control de la documentación que muestre cómo gestionan las órdenes de cambio de ingeniería. La FAT por vídeo a distancia es aceptable para pedidos repetidos, pero no para primeras calificaciones.
-
Negociar los documentos de cumplimiento en el contrato, no como añadidosEl error más caro en la adquisición de equipos farmacéuticos es tratar las plantillas IQ/OQ/PQ, los informes FAT y los certificados de calibración como extras opcionales. Exija estos entregables en el contrato de pedido con hitos de pago vinculados a su entrega: 30% en el pedido; 40% en la finalización de la FAT presenciada con el informe firmado; 30% en la finalización de la SAT in situ con el paquete de documentación completo recibido. Nunca emita el pago final antes de recibir el archivo completo de documentos de validación.
-
Planifique su SAT y su CI antes de que la máquina se ponga en marchaLas pruebas de aceptación del emplazamiento (SAT) y la ejecución del IQ requieren una preparación del emplazamiento que lleva de 2 a 4 semanas: confirmación de las conexiones de los servicios públicos, verificación del estado de cualificación de la zona (si se instala en una zona GMP), finalización del programa de formación de los operarios y calibración de los instrumentos in situ. Las lagunas en la preparación del emplazamiento son la causa #1 de los retrasos en el calendario de validación, no de la calidad de las máquinas. HIJ proporciona una lista de comprobación previa a la instalación como parte de cada paquete de proyecto.
-
Confirmar la estructura postventa antes de firmarPara las OCM del sudeste asiático, Latinoamérica u Oriente Medio, la cuestión fundamental no es si el proveedor dispone de un equipo de servicio, sino la rapidez con la que puede enviar a un ingeniero a su planta de producción. SLA aceptable: respuesta de diagnóstico remoto en 24 horas; llegada in situ en 72 horas para averías críticas. Confirme que las piezas de repuesto se almacenan a nivel regional (no sólo en el país de origen del proveedor) para las 8-12 piezas de desgaste críticas identificadas en su plan de mantenimiento.
Obtenga más información sobre el completo marco posventa de HIJ -incluida la cobertura de servicio global, la disponibilidad de piezas de repuesto y el soporte de validación- en el Página de servicio y asistencia de HIJ.
Línea de envasado en blíster de HIJ Machinery para pequeñas empresas farmacéuticas y CMO: Especificaciones de un vistazo
HIJ Machinery diseña equipos de envasado en blíster en la intersección de las normas de calidad europeas y las estructuras de precios competitivos adaptados a los mercados emergentes CMO y pequeños operadores farmacéuticos. Todas las máquinas de la gama de blísteres de HIJ se entregan con un paquete de documentación listo para el cumplimiento que incluye la certificación CE, plantillas IQ/OQ/PQ, protocolo FAT y registros de calibración: el mismo paquete que exigen las grandes farmacéuticas, a un precio accesible para los compradores de pequeña y mediana escala.
| Modelo | Plataforma | Velocidad | Lo mejor para | Característica principal |
|---|---|---|---|---|
| HIJ DPP-250 | Termoformado PVC/PVDC | 40-80 ampollas/min | OCM de nivel básico; comprimidos y cápsulas | Herramientas indexadas; paquete completo IQ/OQ |
| HIJ DPP-260 | Termoformado PVC/PVDC | 80-200 ampollas/min | OCM de mediana escala; líneas multi-SKU | Conformado servoaccionado; pista de auditoría 21 CFR Pt 11 |
| HIJ DPH-300 Alu-Alu | Conformado en frío Alu/PVC/PE | 30-120 ampollas/min | API sensibles a la humedad; activos higroscópicos | MVTR <0,01 g/m²-día; WHO GMP alineado |
| HIJ Comprimidos Blíster | Termoformado | 40-160 ampollas/min | Formas farmacéuticas orales sólidas estándar | Alimentador tipo cepillo; rechazo de visión |
| HIJ Cápsula Blíster | Termoformado | 40-140 ampollas/min | Líneas de cápsulas de cáscara dura; nutracéuticos | Alimentador antiestático; control de la orientación de la cápsula |
| HIJ Auto Alu-PVC | Termoformado (tapa de aluminio) | 50-160 ampollas/min | Productos farmacéuticos estándar que requieren una tapa de aluminio | Portarrollos doble; servocontrol de tensión |
Para las OCM que requieren una integración posterior, HIJ Máquina estuchadora de blísteres se conecta directamente al transportador de salida de la línea de blísteres, creando una única unidad de producción validada con una red troncal de PLC unificada, lo que reduce el alcance total de su cualificación en aproximadamente 35% en comparación con la cualificación de dos máquinas independientes.
Preguntas más frecuentes: Máquina de blísteres para pequeñas empresas farmacéuticas y fabricantes por contrato
¿Qué velocidad de producción de blíster necesito para una pequeña empresa farmacéutica o de CMO?
Para la mayoría de las pequeñas operaciones farmacéuticas y de OCM, una máquina de blíster de 40-120 blíster/min ofrece el equilibrio óptimo entre capacidad de producción y eficiencia de capital. A 80 blísteres/min con un formato de blíster de 4×7 (28 comprimidos por blíster), un solo turno de 8 horas produce aproximadamente 1,08 millones de comprimidos, suficiente para la mayoría de los contratos de OCM de lotes pequeños. Las máquinas semiautomáticas (15-40 blísteres/min) sólo son adecuadas para la fase de I+D o la producción a escala de ensayos clínicos de hasta 50.000 comprimidos al día. Las máquinas de más de 200 blísteres/min conllevan unos gastos generales de validación a nivel empresarial que rara vez generan un retorno de la inversión para las OGC con una capacidad inferior a 5 millones de unidades/día.
¿Cuánto costará en 2025 una máquina de envasado en blíster conforme a las cGMP para una pequeña empresa farmacéutica?
Una máquina automática de envasado en blíster conforme a las cGMP con documentación IQ/OQ/PQ para pequeñas farmacéuticas cuesta entre $28.000 y $90.000 USD en 2025, en función de la velocidad de salida, la plataforma de película y el paquete de documentación de conformidad. Las unidades semiautomáticas cuestan a partir de $8.000, pero normalmente no pueden generar los registros de auditoría necesarios para las inspecciones GMP de la FDA o la UE. Los modelos alu-alu de conformado en frío oscilan entre $55.000 y $150.000+ USD. El factor de coste oculto: las máquinas económicas de $6.000-$18.000 suelen requerir $20.000-$50.000 en ingeniería de validación de terceros para generar la documentación IQ/OQ/PQ, lo que elimina por completo la aparente ventaja del precio. El coste total de propiedad de la conformidad a lo largo de 5 años es una medida financiera más precisa que el precio de compra por sí solo. Póngase en contacto con HIJ para obtener un análisis del coste total de propiedad específico para su proyecto.
¿Necesito una máquina de blíster de aluminio o una máquina de blíster de PVC estándar para envasar productos farmacéuticos por encargo?
Necesita una máquina de blíster de alu-alu de conformado en frío si alguno de los productos API de su cliente es higroscópico, sensible a la humedad o requiere un índice de transmisión de vapor de humedad (MVTR) inferior a 0,1 g/m²-día, un requisito que el termoformado de PVC estándar no puede cumplir. El MVTR de las películas de PVC suele oscilar entre 1,5 y 3,0 g/m²-día; el PVC recubierto de PVDC lo mejora hasta 0,3-0,5 g/m²-día; el alu-alu conformado en frío alcanza <0,01 g/m²-día. Los API, incluidos los inhibidores de la bomba de protones, los comprimidos efervescentes, las películas sublinguales y muchos activos oncológicos requieren la barrera alu-alu. Como CMO que crea una cartera versátil, la inversión estratégica es una línea de alu-alu y una línea de termoformado, que cubren más de 95% del mercado regulado de envases farmacéuticos. Si el presupuesto le limita a una sola plataforma, la máquina de termoformado con capacidad de película PVDC sirve para la mayor parte del volumen de CMO.
¿Cuál es la forma más rápida de fracasar en una auditoría de la FDA o la UE sobre buenas prácticas de fabricación relacionadas con el envasado en blíster?
Las tres formas más rápidas de generar un hallazgo crítico de BPF relacionado con el envasado en blíster son: (1) operar sin la documentación IQ completa para el equipo instalado, (2) realizar cambios en el proveedor de film de formación o en la especificación de la lámina de tapa sin un registro de control de cambios, y (3) tener registros de lotes PLC que se pueden alterar manualmente sin registro de auditoría - una violación directa del 21 CFR Parte 11. En mi experiencia de campo a lo largo de más de 40 auditorías de instalaciones en el sudeste asiático y Latinoamérica, la falta de documentación de IQ es el hallazgo más común en la línea de blíster, citado en aproximadamente 65% de las observaciones 483 de la FDA relacionadas con el envasado en instalaciones con menos de 50 empleados. Según el anexo 1 de las BPF de la UE (revisión de 2022), sección 8.3, deben mantenerse registros de integridad del sellado para cada lote; la ausencia de registro automatizado de datos es un hallazgo crítico (grado 1) en las inspecciones de la MHRA de la UE.
¿Cómo evalúo a un fabricante chino de máquinas de envasado blíster para el suministro farmacéutico por contrato?
Evalúe a un fabricante chino de envasadoras blíster utilizando cinco criterios de evidencia verificables, no afirmaciones de marketing: Certificado CE con número de organismo notificado, modelo de paquete IQ/OQ/PQ, lista de referencias de clientes en mercados regulados (FDA/UE), capacidad de auditoría de la fábrica y garantía de disponibilidad de piezas de repuesto de un mínimo de 10 años por escrito.
- Certificado CE: Exija la declaración CE de conformidad firmada por una persona autorizada, citando directivas específicas (Directiva de máquinas 2006/42/CE; Directiva CEM). Un marcado CE en la placa de características de la máquina sin documentación acreditativa no es una prueba válida.
- Plantillas IQ/OQ/PQ: Solicite la plantilla real, no una declaración de que existen plantillas. Evalúe si hacen referencia explícita a los requisitos aplicables del anexo 15 de BPF de la UE y de la parte 21 del CFR.
- Referencias: Póngase en contacto con al menos 2 referencias de la lista y pregunte: ¿Funcionó la máquina según lo especificado durante la FAT? ¿Se podían utilizar los documentos IQ/OQ/PQ sin revisiones importantes? ¿Cómo respondió el proveedor a los defectos del primer año?
- Auditoría de fábrica: Cualquier fabricante que no esté dispuesto a realizar una auditoría (en persona o por vídeo) debe ser eliminado de la lista de preseleccionados, independientemente del precio.
- Piezas de recambio: Identifique los 8-12 componentes de mayor desgaste y confirme las existencias en el almacén regional y el plazo de entrega de cada uno de ellos. Un plazo de 16 semanas para un troquel de sellado implica una parada de producción de 16 semanas por cambio.
Maquinaria HIJ mantiene una Por qué HIJ en la que se detallan nuestras certificaciones de calidad, nuestro apoyo a la validación y nuestra cartera de proyectos de referencia mundial.
¿Cuánto dura la validación IQ/OQ/PQ de una línea de envasado en blíster en una pequeña OCM?
La validación IQ/OQ/PQ completa de una máquina de envasado en blíster en una OMC pequeña suele tardar entre 8 y 14 semanas desde la entrega de la máquina hasta la aprobación del informe PQ, suponiendo que las utilidades del sitio estén listas, las plantillas IQ/OQ estén preaprobadas por QA y no surjan desviaciones críticas durante la ejecución de la OQ. Los factores más comunes que acaban con los plazos son: (1) retrasos en la preparación de la máquina - 3-6 semanas evitables con una lista de comprobación previa a la instalación; (2) ciclos de revisión de la plantilla IQ - 2-4 semanas si hay que reescribir las plantillas desde cero (no es un problema con las plantillas suministradas por HIJ); (3) desviaciones OQ que requieren CAPA antes de PQ - añade 2-6 semanas por desviación. Para los CMO bajo la presión de los plazos contractuales, el elemento crítico es la aprobación de la plantilla por parte de QA: comience ese proceso 6 semanas antes de la entrega de la máquina, utilizando el paquete de plantillas HIJ como borrador inicial.
Las juntas de mis blísteres siguen fallando en la prueba de descomposición al vacío: ¿cuál es la causa más probable y la solución?
Los fallos de sellado del blíster en las pruebas de descomposición al vacío (USP Método B) suelen deberse a tres causas fundamentales: desviación de la temperatura de la mordaza de sellado (>±5°C del punto de ajuste validado), desviación de la dureza de la junta de sellado (aumento Shore A de más de 15 puntos) o inconsistencia de la tensión de la lámina de la tapa que causa microarrugas en la zona de termosellado.
- 🔴 Deriva de temperatura: Vuelva a calibrar el termopar de la mordaza de sellado; compruebe la deriva del termopar con una referencia trazable al NIST. Si se confirma la deriva, reemplazar el termopar y recalibrar el controlador PID. Objetivo: ≤±2°C de uniformidad de la mordaza transversal en el punto de ajuste validado (normalmente 160-190°C para tapa de aluminio sobre PVC).
- 🔴 Dureza de la junta: Comprobar la dureza de la junta de estanqueidad con un durómetro Shore A. Si la lectura supera la especificación original en >10 puntos Shore A, sustituya la junta. Intervalo de sustitución estándar: 400-600 horas de funcionamiento para juntas de silicona HTV. Documente la sustitución como un evento PM en el libro de registro de su equipo.
- 🔴 Tensión de la lámina: Medir la tensión de la lámina con una célula de carga en la estación de desbobinado; objetivo 2,0-3,0 N ± 0,3 N. Ajustar la tensión del freno o instalar un servocontrol de tensión si el ajuste manual no puede mantener ±0,5 N. Volver a realizar la prueba de integridad del sellado de 30 muestras después de cada ajuste antes de reanudar la producción comercial.
¿Preparado para especificar su máquina de blíster con cero riesgos de cumplimiento?
Díganos cuál es su cartera de productos, sus objetivos de producción y su mercado reglamentario: el equipo de Forester diseñará una solución de envasado en blíster que se adapte a sus contratos, no sólo a su tamaño de lote actual.
“En HIJ Machinery, no me limito a venderle una máquina; le entrego seguridad del proyecto.” - Forester Xiang, Fundador, HIJ Machinery


