Блистерная машина для Малая фармацевтика и контрактные производители: Определяющее руководство покупателя
Выбор неправильного блистерная машина для малого фармацевтического производства не просто стоит вам капитала - она стоит вам готовности к аудиту, скорости перехода на новый формат и, в конечном счете, контрактов, обеспечивающих ваш рост. Это проверенное на практике руководство поможет вам с первого раза сделать правильный выбор.
По словам Форестера Сяна, основателя компании HIJ Machinery с 20-летним опытом работы на производственных площадках от Боготы до Бангкока: ОКУ, приобретающие блистерные упаковщики без документации IQ/OQ, сталкиваются с расходами на повторную квалификацию, которые в среднем составляют 3× первоначальных инвестиций в оборудование при проведении аудита в соответствии с FDA 21 CFR Part 211 или EU GMP Annex 1 (пересмотр 2022 года).
👤 Проницательность лесника
20-летняя перспектива развития отраслиПрямой ответ: Для небольших фармацевтических компаний и контрактных производителей правильная машина для блистерной упаковки - это не самая дешевая машина, а та, которая Масштабируется в соответствии с портфелем контрактов, не вызывая дорогостоящего восстановления соответствия требованиям каждый раз, когда меняется ваш SKU.
Полевой опыт и скрытая ловушка: За 20 лет работы на производственных площадках от Боготы до Бангкока я наблюдал, как бесчисленное множество ОКУ закупают недорогие автономные блистеры с нулевой документацией cGMP, а спустя несколько месяцев проваливают аудит FDA или Приложения 1 ЕС, что влечет за собой затраты на повторную сертификацию, которые втрое превышают их первоначальные инвестиции. Скрытая ловушка, о которой вас никто не предупреждает: Бюджетные машины редко поставляются с протоколами IQ/OQ или надлежащей поддержкой FAT/SAT., В результате ваша команда будет вынуждена писать валидационные документы в условиях давления со стороны регулирующих органов.
Стратегический совет: Прежде чем подписывать любой контракт, требуйте полного анализа URS и подтвердите, что поставщик может поддерживать валидацию смены формата для нескольких типов продуктов, а не только для демонстрационного планшета. В HIJ наша философия интеграции "под ключ" означает, что малые и средние предприятия получают ту же инженерную базу, соответствующую требованиям cGMP, что и крупные производители, но без ценника предприятия. Приобретайте соответствие один раз, масштабируйте уверенно.
Идеал блистерная машина для упаковки блистеров в малые фармацевтические препараты и контрактные фармацевтические препараты это термоформовочный или алюмокалиевый блистерный упаковщик производительностью 30-120 блистеров/мин, Поставляется с полной документацией IQ/OQ/PQ, комплектами оснастки разных форматов и контрольным журналом на базе ПЛК, соответствующим 21 CFR Part 11. Документация по соответствию не подлежит обсуждению - оборудование без нее не пройдет инспекцию FDA или EU GMP Annex 1 (2022), что приведет к расходам на повторную валидацию, которые обычно превышают $80,000 долларов США за цикл аудита.

Термоформовочная машина для блистерной упаковки HIJ DPP-250 - идеальное решение для небольших фармацевтических предприятий, требующих соблюдения требований cGMP и гибкости в использовании нескольких форматовSKU.
Почему выбор блистерной машины - это решение о соответствии требованиям, а не просто решение о капитальных затратах для малых фармкомпаний и ОКУ
Контрактная линия блистерной упаковки для фармацевтической промышленности должна одновременно выполнять две задачи: производить продукцию с приемлемой экономичностью и удовлетворить требования регуляторов, которые следуют за каждым новым контрактом с клиентом. Небольшие фармпроизводители и CMO - обычно работающие с 2-8 SKU с объемом производства от 30 000 до 500 000 блистеров в день - сталкиваются с принципиально иной системой выбора, чем крупносерийные производители, работающие с одним продуктом 24/7.
Основная операционная реальность: блистерная машина CMO должна выполнять подтвержденную смену формата менее чем за 30 минут, чтобы оставаться прибыльной при переходе от одного продукта к другому. Каждый комплект оснастки (формовочная форма, штамп для запечатывания, вырубной штамп) должен быть задокументирован, контролироваться по версиям и отслеживаться в соответствии с требованиями ВОЗ TRS 992 Приложение 3 и ЕС GMP Приложение 15 к реквалификации. Машина, обеспечивающая производительность 200 блистеров в минуту, но требующая 4 часа непроверенной переналадки, - это пассив, а не актив.
В сегменте малых фармацевтических компаний и CMO преобладают три конфигурации оборудования. Каждая из них влечет за собой определенные последствия для соблюдения нормативных требований:
Полуавтоматический блистерный упаковщикПроизводительность: 15-40 блистеров/мин. Низкая первоначальная стоимость ($8 000-$28 000 долларов США). Ограниченные возможности аудита. Подходит для ОКУ на этапе НИОКР с производительностью <50 000 единиц продукции в день. Как правило, требуется дополнительная валидационная документация.
Автоматическая термоформовка (ПВХ/PVDC)Производительность: 40-200 блистеров/мин. Средняя стоимость ($25,000-$90,000 USD). Полный контрольный журнал PLC. Стандартная в отрасли платформа для таблеток, капсул и пилюль. Самый гибкий профиль смены форматов.
Блистеры холодной формовки Alu-AluПроизводительность: 30-120 блистеров/мин. Более высокая удельная стоимость ($55 000-$150 000+ долларов США). Обязателен для чувствительных к влаге API, требующих барьера MVTR 0,01-0,1 г/м²-день. Требуется в соответствии с Приложением 1 к GMP ЕС для нескольких категорий контролируемых веществ.
Вызов для CMO с несколькими продуктами: почему проверка смены формата - это ваша спецификация #1
Один раз проверьте машину для продукта А. Теперь ваш новый клиент требует продукт Б с другим диаметром таблеток (12 мм против 9 мм), другим форматом блистера (4×7 против 3×5) и с покрытием PVDC вместо алюминиевой фольги. Без машины, предназначенной для быстрой и документированной переналадки, вам придется пройти полный цикл переквалификации в соответствии с приложением 15 к GMP ЕС, что обойдется в 3-6 недель и $15 000-$40 000 за одно изменение в зависимости от вашего регуляторного рынка. Установки HIJ серий DPP-250 и DPP-260 оснащены механизмами фиксации оснастки, которые позволяют документировать переналадку в формате менее чем за 2 часа, используя пронумерованные наборы оснастки, которые непосредственно соответствуют журналу отклонений URS.

Для операций по производству блистерной упаковки в соответствии с требованиями cGMP требуется как возможность аудиторского контроля на стороне машины, так и протоколы документации оператора - и то, и другое должно быть указано в вашем URS.
Распространенные неисправности и их устранение - этап выбора машины
- 🔴 Симптом: CMO приобретает недорогой блистерный упаковщик; через 8 месяцев он не проходит аудит по приложению 1 GMP ЕС из-за отсутствия журнала температурного режима запечатывания и недостаточной документации по IQ.
⚙️ Коренная причина: ПЛК машины использует собственный, неэкспортируемый формат данных, не имеющий аудиторского следа в соответствии с 21 CFR, часть 11. Контроллер температуры уплотнительных губок не имеет возможности отслеживания калибровки (дрейф допуска >±5°C не обнаружен).
🔧 Фикс Форестера: Закажите как минимум ПЛК Siemens S7-1200 или Allen-Bradley ControlLogix с возможностью экспорта записей о партиях в формате CSV. Допуск на температуру уплотнительных губок должен составлять ≤±2°C с 4-часовым протоколированием калибровочного цикла. Подтвердите наличие шаблона IQ/OQ до подписания PO. - 🔴 Симптом: Переход с формата блистера 10×1 на формат блистера 5×2 занимает более 6 часов; CMO теряет $12 000 производственного времени на переходе.
⚙️ Коренная причина: Комплекты оснастки не нумеруются и не контролируются по версиям; выравнивание пресс-форм требует ручной подгонки без точек отсчета повторяемости.
🔧 Фикс Форестера: Требуются станки с индексируемыми держателями оснастки (выравнивание по штифтам) и серийными номерами оснастки, нанесенными лазером, которые соответствуют утвержденному каталогу сменных деталей. Целевое время переналадки: <45 минут от последнего хорошего блистера до первого хорошего блистера нового формата, полностью документированного. - 🔴 Симптом: Нарушения целостности герметизации при 15-18% на производственных площадках с влажным климатом (Юго-Восточная Азия, Латинская Америка), что привело к отзыву продукции.
⚙️ Коренная причина: Распределение тепла на станции запечатывания неравномерно по ширине губок (разница >8°C от центра к краю); недостаточный контроль натяжения фольги, вызывающий появление микроморщин на пленке.
🔧 Фикс Форестера: Закажите многозонный контроль температуры запечатывания с равномерностью ≤3°C в поперечном направлении. Сервоуправление натяжением фольги (регулируемое усилие 0,5-5,0 Н) предотвращает сморщивание крышки. Удостоверьтесь в соответствии с ASTM F2338 (неразрушающие испытания целостности упаковки) с помощью записей испытаний на разрушение вакуума 100%.
Критические технические условия для контрактных машин для блистерной упаковки фармацевтической продукции: Что должна содержать ваша URS
Разработка спецификации блистерного упаковщика без спецификации требований пользователя (URS) - это самый быстрый путь к провалу цикла квалификационной оценки (IQ/OQ/PQ). URS увязывает ваши нормативные обязательства с техническими возможностями машины, а для ОКУ она должна учитывать максимально широкий портфель продукции, а не только список ваших текущих клиентов. Приведенные ниже 9 технических параметров представляют собой минимальную жизнеспособную спецификацию для любой блистерной машины фармацевтического класса, предназначенной для рынков, регулируемых FDA или EU GMP.
Термоформование и холодная формовка алюмооксида: Выбор правильной платформы для вашего портфеля API
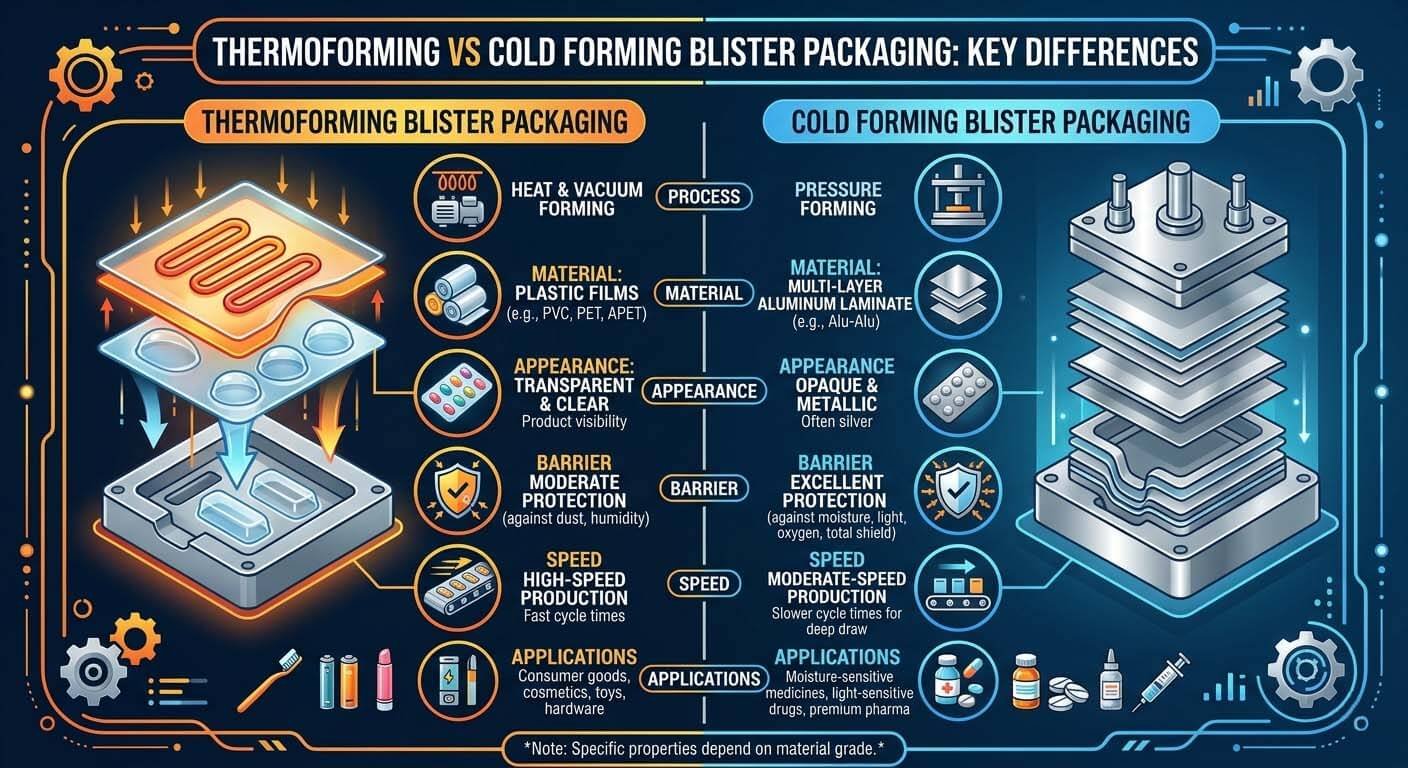
Термоформование (PVC/PVDC) против холодной формовки Alu-Alu: разница в барьерных характеристиках определяет, какая платформа нужна вашему портфелю API.
| Параметр | Термоформование HIJ (DPP-250/260) | HIJ Холодная штамповка Alu-Alu (DPH-300) | Бюджетные машины |
|---|---|---|---|
| Выходная скорость | 40-200 волдырей/мин | 30-120 волдырей/мин | 20-80 волдырей/мин |
| Формовочная пленка | ПВХ, ПВДК, ПВХ/ПЕ, ПП | Alu/PVC/PE (фольга для холодного формования) | Только ПВХ (большинство моделей) |
| Барьер от влаги (MVTR) | 0,3-3,0 г/м²-день (PVDC) | <0,01 г/м²-день (превосходно) | Неуказанный / не включенный в список |
| Контроль температуры уплотнения | Многозонный ±2°C | Многозонный ±2°C | Однозонный ±8-15°C |
| ПЛК / контрольный журнал | Siemens S7 / Allen-Bradley; готовность 21 CFR Pt 11 | Siemens S7 / Allen-Bradley; готовность 21 CFR Pt 11 | Собственная разработка; функция экспорта отсутствует |
| Документы IQ/OQ/PQ | Полные шаблоны FAT/SAT + IQ/OQ/PQ | Полные шаблоны FAT/SAT + IQ/OQ/PQ | Нет в стандартной комплектации; оплачивается дополнительно |
| Переключение форматов | <45 мин при использовании индексированной оснастки | <60 минут с индексированной оснасткой | 3-8 часов; повторяемость отсутствует |
| CE / WHO GMP | Сертифицировано CE; соответствует GMP ВОЗ | Сертифицировано CE; соответствует GMP ВОЗ | Заявлено CE; документация отсутствует |
| Испытание на целостность уплотнения | Совместимость с ASTM F2338 / USP | Совместимость с ASTM F2338 / USP | Только визуально; никаких данных по приборам |
| Диапазон цен (USD) | $28,000–$75,000 | $55,000–$130,000 | $6,000–$22,000 |
Изучите полный Линия продукции блистерной упаковочной машины HIJ В том числе термоформовочные, алюмокалиевые, жидкостные и капсульные блистеры - все они разработаны в соответствии со стандартами cGMP.
9 необсуждаемых параметров URS для оборудования для блистерной упаковки CMO
- Равномерность температуры уплотнительных губок ≤±2°C - Отклонение температуры челюсти на 12°C приводит к снижению целостности печати по ширине блистера на 40%, согласно данным проверки ASTM F2338. Обязательно наличие многозонного ПИД-регулирования.
- Электронные записи партий, соответствующие требованиям 21 CFR, часть 11 - Требуются журналы данных с временными метками, с присвоением оператору, с гарантией вскрытия для каждого производственного цикла. Экспорт данных в формате CSV или SQL обязателен для представления в регулирующие органы.
- Подтвержденное время переключения ≤60 минут для всех комбинаций форматов, задокументированных в вашем каталоге продукции - измеряется от последнего хорошего блистера (формат A) до первого хорошего блистера (формат B), полностью отслеживается.
- Спецификация MVTR для формовочной пленки - Минимум: ПВХ ≤3,0 г/м²-день; PVDC ≤0,3 г/м²-день; алю-алю ≤0,01 г/м²-день. Должно быть подтверждено сертификатом анализа поставщика пленки в DHF.
- Система отбраковки с контролем полости 100% - Обнаружение пустых полостей с помощью камеры или весов с автоматическим отбраковыванием; события отбраковки регистрируются в протоколе партии в соответствии с 21 CFR Part 211 Subpart K.
- Контактные поверхности из нержавеющей стали класса GMP - SS 316L для всех деталей, контактирующих с продуктом; обработка поверхности Ra ≤0,8 мкм; сварные швы без трещин в соответствии со стандартом ASME BPE.
- Протокол FAT (заводских приемо-сдаточных испытаний) - Минимальный 4-часовой испытательный пробег на заданной скорости с коэффициентом дефектности <0,5%; все функции сигнализации и блокировки безопасности проверены и задокументированы.
- Пакет шаблонов IQ/OQ/PQ - Предоставленные поставщиком мастер-шаблоны, согласованные с требованиями к фармацевтическим системам качества EU GMP Annex 15 и ICH Q10. Шаблоны должны быть редактируемыми и настраиваемыми для конкретного объекта.
- Гарантия наличия запасных частей - минимум 10 лет - Подтверждено в письменном виде, включая критические быстроизнашивающиеся детали: пресс-форму, уплотнительную матрицу, вырубной инструмент, уплотнительную прокладку, кулачковый механизм.
Приложение 15 к GMP ЕС
21 CFR, часть 211
21 CFR, часть 11
ИВВ ВОЗ 992 Приложение 3
ICH Q10
ASTM F2338
USP
ISO 13849-1
Распространенные способы устранения неисправностей и исправления Forester's - Фаза технической спецификации
- 🔴 Симптом: Блистерная печать не проходит тест на вакуумное разрушение (USP Method B) с показателем дефектности 8% после 3 месяцев эксплуатации - аудитор отмечает критическое отклонение в соответствии с 21 CFR Part 211.134.
⚙️ Коренная причина: Твердость уплотнительной прокладки изменилась с 55 до 72 единиц по Шору A в результате циклического воздействия тепла; в сочетании с несоответствием натяжения пленки (измерено ±18%), что привело к появлению дефектов уплотнения микроканалов, невидимых при визуальном осмотре.
🔧 Фикс Форестера: Внедрите график 500-часового ТО для замены уплотнительных прокладок. В качестве материала для прокладок указать силикон (сорт HTV, твердость по Шору A 50-60 при рабочей температуре). Установите тензодатчик натяжения фольги (целевое значение: 2,5 Н ± 0,3 Н) с регистрацией партии в режиме реального времени. После каждой смены прокладки проводите повторную квалификацию в соответствии с USP Method B. - 🔴 Симптом: Таблетки разломились в 3-5% блистерах при высокоскоростном формовании при скорости 160 блистеров в минуту; жалоба клиента вызвала замечание FDA 483.
⚙️ Коренная причина: Температура формовочной плиты 180°C на пленке ПВХ, рассчитанной на 155-165°C; слишком размягченная пленка частично разрушается под весом таблетки во время переноса полости, вызывая ударные трещины по краям таблетки.
🔧 Фикс Форестера: Перекалибруйте формовочную станцию до 158°C ± 2°C для пленки ПВХ толщиной 250 мкм. Проверьте с помощью ИК-термометра по всей ширине формования (9 точек измерения). Включите отбраковку подсчета таблеток для частичных блистеров; регистрируйте все случаи отбраковки в соответствии с 21 CFR Part 211. - 🔴 Симптом: Записи о партиях ПЛК невозможно экспортировать или распечатать в формате, пригодном для аудита - инспектор FDA выдает 483 замечание за несоответствие требованиям 21 CFR, часть 11.
⚙️ Коренная причина: Машина поставляется с собственным сенсорным экраном HMI, который хранит данные в двоичном формате; нет возможности экспорта через USB или подключения к сети; нет ролевого управления доступом или возможности электронной подписи.
🔧 Фикс Форестера: Укажите ПЛК Siemens S7-1500 или Allen-Bradley ControlLogix с интерфейсом SCADA WinCC. Требуется: (1) ролевой логин с минимум 3 уровнями доступа, (2) экспорт CSV с цифровой контрольной суммой, (3) минимальный срок хранения локальных данных 30 дней, (4) документ матрицы соответствия 21 CFR Part 11, предоставленный поставщиком до получения заказа.
Валидация IQ/OQ/PQ для линий блистерной упаковки CMO: Что должен предоставить ваш поставщик
Валидация - это процесс, с помощью которого ваша команда - и регуляторный орган - подтверждают, что блистерная машина постоянно производит продукцию, соответствующую заданным спецификациям качества. Для ОКУ, работающих по контрактным соглашениям на поставку блистерной упаковки для фармацевтической промышленности, бремя валидации усиливается: каждый новый продукт клиента обычно вызывает событие повторной валидации, а машина, которая не была разработана для документированной переналадки, приведет к затратам на валидацию, которые уничтожат маржу вашего проекта в течение 18 месяцев.
Последовательность DQ → IQ → OQ → PQ не является бюрократическим излишеством - это защита вашей ответственности. Согласно Приложению 15 к GMP ЕС (2015) и 21 CFR Part 211 Subpart J, отсутствие или неполная запись IQ (Installation Qualification) делает каждую последующую партию, произведенную на этом оборудовании, потенциально не подлежащей повторному выпуску. Вот что необходимо документировать на каждом этапе линии блистерной упаковки:

Жизненный цикл валидации DQ → IQ → OQ → PQ: каждая машина для блистерной упаковки, поступающая на регулируемое предприятие CMO, должна пройти эту последовательность до выпуска коммерческой партии.
Дорожная карта валидации DQ → IQ → OQ → PQ для оборудования для блистерной упаковки
-
DQ - Design Qualification: Заблокируйте URS перед заказомПеред покупкой документально подтвердите, что конструкция оборудования соответствует вашим нормативным и эксплуатационным требованиям. Результаты DQ: заполненная URS, контрольный список DQ поставщика, подписанный квалифицированным специалистом, оценка рисков в соответствии с ICH Q9, охватывающая целостность уплотнений, материалы, контактирующие с продуктом, и целостность данных. Подтвердите здесь решение о применении алюмооловянной или термоформовочной платформы - смена платформы после DQ влечет за собой полную ревалидацию.
-
FAT - заводские приемочные испытания: Квалификация на заводе поставщикаПроведите засвидетельствованный, минимум 4-часовой производственный цикл на предприятии поставщика с указанной вами скоростью производства. FAT должен включать: тестирование всех аварийных сигналов (низкий уровень пленки, смещение блистера, отклонение температуры >5°C), отбор образцов целостности запечатывания (минимум 30 блистеров каждого формата), демонстрацию переналадки для каждого комплекта оснастки в вашем каталоге продукции и проверку экспорта данных. HIJ включает шаблоны протоколов FAT в стандартную комплектацию; требуйте подписанный отчет FAT в качестве предварительного условия для окончательной оплаты.
-
IQ - квалификация установки: Документируйте то, что было доставлено, и то, как это было установленоУбедитесь, что установленное оборудование соответствует утвержденной проектной спецификации. Контрольный список IQ включает: перекрестную ссылку серийного номера оборудования на PO, проверку подключения к инженерным сетям (сжатый воздух: 6-8 бар ±5%; электричество: 380 В/50 Гц ±3%), подтверждение чистоты поверхности GMP (SS316L, Ra ≤0,8 мкм), сертификаты калибровки для всех приборов (термопара, манометр, тензодатчик), блокировку версии программного обеспечения с контрольной суммой и запись чертежа установки в соответствии со строительными требованиями. IQ должен быть рассмотрен и подписан специалистом по контролю качества на вашем предприятии и инженером по установке поставщика.
-
OQ - эксплуатационная квалификация: Испытание каждой функции на пределе возможностейПродемонстрируйте, что машина работает в соответствии со спецификацией во всем рабочем диапазоне, а не только при номинальной уставке. OQ для блистерных упаковщиков должен включать: испытание температуры запечатывания при ±5°C от номинальной уставки (подтверждение целостности запечатывания при обоих крайних значениях), испытание в диапазоне скоростей от 20% до 100% номинальной производительности, испытание точности отбраковки пустых полостей (впрысните 50 намеренно пустых полостей; подтвердите показатель отбраковки 100%), функциональное испытание сигнализации и блокировки для всех 12-20 перечисленных сигнализаций и 4-часовую непрерывную работу на номинальной скорости с OEE ≥92%.
-
PQ - квалификация производительности: Три последовательные проверенные партииПроизведите 3 последовательные коммерческие партии вашего первого зарегистрированного продукта, каждая из которых должна соответствовать всем заранее установленным критериям приемки. Критерии приемки PQ должны включать: целостность уплотнения в соответствии с USP Method B (целевой уровень дефектов 0%; максимальный уровень AQL 0,1%), равномерность веса в пределах ±3% от номинального веса таблетки на полость, полноту записи партии (заполненные поля 100%, отсутствие ручных исправлений без подписанного журнала отклонений) и производительность переналадки для каждого дополнительного формата в каталоге валидированной продукции.
-
Текущая работа: Ежегодная переквалификация и контроль измененийЛюбое изменение поставщика формовочной пленки, спецификации пленки для укупоривания, комплекта оснастки, версии программного обеспечения ПЛК или материала уплотнительной прокладки влечет за собой пересмотр контроля изменений в соответствии с разделом 13 Приложения 15 к EU GMP. Классифицируйте каждое изменение как незначительное (только уведомление), умеренное (частичная переквалификация затронутых функций) или значительное (полное повторение OQ/PQ). Включите это в график профилактического обслуживания с интервалом не менее 12 месяцев.
Для ОКУ, рассматривающих возможность создания полностью интегрированной линии по производству блистеров и коробок с единой основой для валидации, следует изучить Упаковочные решения HIJ под ключ - разработаны для минимизации общей нагрузки по проверке всего комплекса вторичной упаковки.
Распространенные способы отказа и их устранение - фаза выполнения валидации
- 🔴 Симптом: OQ терпит неудачу в тесте на отбраковку пустых полостей - 4 из 50 намеренно пустых блистеров проходят незамеченными, что приводит к критическому отклонению OQ, которое останавливает валидацию на 6 недель.
⚙️ Коренная причина: Порог чувствительности системы контроля камеры установлен слишком широко (зона обнаружения охватывает только 60% глубины полости); полузаполненная полость с фрагментом таблетки проходит порог.
🔧 Фикс Форестера: Перенастройте зону обнаружения системы технического зрения так, чтобы она охватывала 95% объема полости (настройте маску ROI в HMI). Установите порог отбраковки резервных копий на основе веса на ≥±15% от номинального веса таблетки. Повторно провести тест на впрыск 50 полостей; задокументировать как отклонение OQ в CAPA. Цель: 0/50 отбраковок до повторной квалификации. - 🔴 Симптом: PQ Batch 2 не прошла проверку полноты записи партии - обнаружено 12 ручных записей без журнала отклонений, что отмечено как потенциальное нарушение целостности данных в соответствии с принципами ALCOA+.
⚙️ Коренная причина: Пробел в обучении операторов - персонал не знает, что любое ручное изменение уставки ПЛК должно регистрироваться как событие, связанное с отклонением, а не просто отмечаться в журнале.
🔧 Фикс Форестера: Внедрите ролевую блокировку HMI, которая заставляет заполнять форму обязательного ввода отклонений при ручном изменении уставки за пределами ±5% от утвержденного диапазона. Обучить всех операторов требованиям ALCOA+ (атрибутируемость, разборчивость, современность, оригинальность, точность + полнота, последовательность, долговечность). Выдать CAPA; повторно запустить партию PQ 2 после подтверждения закрытия CAPA в течение 30 дней.
Пошаговый процесс покупки: Как малые фармацевтические компании и ОКУ должны оценивать и выбирать машину для блистерной упаковки
Решения о закупках оборудования для блистерной упаковки остаются необратимыми в течение 10-15 лет. Структурированный процесс поиска поставщиков позволяет избежать трех наиболее распространенных ошибок при закупках: покупка сегодняшних мощностей, а не завтрашнего портфеля контрактов, занижение требований к документации о соответствии и выбор поставщиков, которые исчезают после ввода в эксплуатацию. Эта 7-ступенчатая схема основана на непосредственном опыте Forester по отбору поставщиков для клиентов CMO из Юго-Восточной Азии, Латинской Америки и Ближнего Востока.
-
Составьте карту всего портфеля продуктов, а не только текущих SKU.Перечислите все виды продукции, которые могут потребоваться вам по соглашению с CMO в течение следующих 5 лет: размеры таблеток (6-22 мм), капсул (00-5), форматы блистеров, типы пленок (ПВХ, PVDC, алюмооловянная) и рынки регулирования (FDA, ЕС, ВОЗ). Это определяет каталог оснастки и определяет, будет ли термоформование или холодная формовка вашей базовой платформой. Машина, предназначенная только для вашего текущего клиента, в будущем станет вашим "узким местом".
-
Составьте проект URS до обращения к поставщикуПоставщик, получивший URS и ответивший на него возражениями или просьбами о пересмотре, говорит вам что-то важное о своих инженерных возможностях. В вашем URS должны быть указаны: диапазон выходных скоростей, совместимость с формовочной пленкой, допустимый температурный режим запечатывания, марка ПЛК и статус соответствия требованиям 21 CFR Part 11, пакет валидационных документов, целевое время переналадки для каждой пары форматов, а также требования к послепродажной поддержке, включая SLA по времени отклика и срок гарантии на запасные части.
-
Составление списка поставщиков на основе доказательств соответствия требованиям, а не брошюрЗапросите у каждого поставщика, вошедшего в короткий список, следующее: (1) образец шаблона IQ/OQ/PQ для вашей модели машины, (2) референс-лист из 3+ клиентов CMO или фармкомпаний на вашем регуляторном рынке с разрешением на контакт, (3) сертификат CE с номером нотифицированного органа, (4) процедурный документ FAT с указанием параметров испытаний и критериев приемки, (5) матрицу соответствия 21 CFR Part 11. Поставщики, не способные предоставить пункты 1, 3 и 4, должны быть отсеяны независимо от цены.
-
Проведите аудит фабрики - или потребуйте живого видео FATДля инвестиций свыше $30 000 USD аудит завода не является обязательным. Подтверждаем: наличие производственной среды, отвечающей требованиям GMP (закрытая сборочная зона, контролируемая влажность), возможность калибровки приборов для измерения температуры и давления на собственном производстве, наличие реального оборудования, работающего на заданной мощности, с размерами таблеток/капсул вашего продукта (принесите образцы), а также наличие системы управления документацией, показывающей, как они управляют заказами на внесение изменений в конструкцию. Удаленное видео FAT приемлемо для повторных заказов, но не для первых квалификаций.
-
Включите документы о соответствии в контракт, а не в качестве дополнительных условийСамая дорогостоящая ошибка при закупке фармацевтического оборудования - рассматривать шаблоны IQ/OQ/PQ, отчеты FAT и сертификаты калибровки как дополнительные опции. Требуйте включения этих документов в договор PO с привязкой этапов оплаты к их поставке: 30% по PO; 40% по завершению FAT с подписанным отчетом; 30% по завершению SAT на месте с получением полного пакета документации. Никогда не производите окончательный платеж до получения полного пакета документов.
-
Планирование SAT и IQ до отправки машиныПриемочные испытания на объекте (SAT) и выполнение IQ требуют подготовки объекта, которая занимает 2-4 недели: подтверждение подключения к коммуникациям, проверка квалификационного статуса зоны (если установка производится в зоне GMP), составление графика обучения операторов и наличие калибровочных инструментов на объекте. Пробелы в готовности площадки являются причиной #1 превышения сроков валидации, а не качества оборудования. HIJ предоставляет контрольный список готовности площадки перед установкой как часть каждого пакета проекта.
-
Подтвердите структуру послепродажного обслуживания до подписания договораДля ОКУ в Юго-Восточной Азии, Латинской Америке или на Ближнем Востоке решающим вопросом является не наличие у поставщика сервисной службы, а скорость прибытия инженера на ваш производственный участок. Приемлемый SLA: 24-часовое дистанционное диагностическое реагирование; 72-часовое прибытие на место для устранения критических неисправностей. Убедитесь, что запасные части хранятся на региональном складе (а не только в стране поставщика) для 8-12 критических изнашиваемых деталей, определенных в вашем плане технического обслуживания.
Узнайте больше о полной системе послепродажного обслуживания HIJ, включая глобальный охват сервиса, наличие запасных частей и поддержку при проверке, на сайте Страница обслуживания и поддержки HIJ.
Линия блистерной упаковки HIJ Machinery для малых фармацевтических предприятий и ОКУ: Технические характеристики с первого взгляда
Компания HIJ Machinery разрабатывает оборудование для блистерной упаковки на стыке европейских стандартов качества и конкурентоспособных цен, подходящих для ОКУ и небольших фармкомпаний, работающих на развивающихся рынках. Каждая машина из линейки блистерного оборудования HIJ поставляется с готовым пакетом документации, включающим сертификат CE, шаблоны IQ/OQ/PQ, протокол FAT и протоколы калибровки - тот самый пакет, который требуется крупным фармацевтическим компаниям, по цене, доступной для мелких и средних покупателей.
| Модель | Платформа | Скорость | Лучшее для | Ключевая особенность |
|---|---|---|---|---|
| HIJ DPP-250 | Термоформование ПВХ/PVDC | 40-80 волдырей/мин | ОКУ начального уровня; таблетки и капсулы | Индексированная оснастка; полный пакет IQ/OQ |
| HIJ DPP-260 | Термоформование ПВХ/PVDC | 80-200 волдырей/мин | Средние ОКУ; многопрофильные линии | Формование с сервоприводом; контрольный журнал по 21 CFR Pt 11 |
| HIJ DPH-300 Alu-Alu | Холодная штамповка Alu/PVC/PE | 30-120 волдырей/мин | Чувствительные к влаге API; гигроскопичные активные вещества | MVTR <0,01 г/м²-день; GMP ВОЗ выровнен |
| Таблетки HIJ в блистере | Термоформование | 40-160 волдырей/мин | Стандартные твердые пероральные лекарственные формы | Щеточный питатель; отбраковка зрения |
| Блистер с капсулами HIJ | Термоформование | 40-140 волдырей/мин | Линии по производству капсул в твердой оболочке; нутрицевтики | Антистатический питатель; контроль ориентации капсулы |
| HIJ Auto Alu-PVC | Термоформование (алюминиевая крышка) | 50-160 волдырей/мин | Стандартные фармацевтические препараты, требующие фольгированной упаковки | Двухрулонный держатель фольги; сервоуправление натяжением |
Для ОКУ, нуждающихся в интеграции с последующим производством, HIJ Картонировочная машина для блистеров Подключается непосредственно к выходному конвейеру блистерной линии, создавая единый валидированный производственный блок с единой базой ПЛК, что позволяет сократить общий объем квалификации примерно на 35% по сравнению с квалификацией двух отдельных машин.
Часто задаваемые вопросы: Блистерная машина для малых фармацевтических предприятий и контрактных производителей
Какая скорость выпуска блистерной машины мне нужна для небольшой фармацевтической компании или CMO?
Для большинства небольших фармацевтических предприятий и компаний CMO блистерная машина производительностью 40-120 блистеров в минуту обеспечивает оптимальный баланс производственной мощности и капиталоотдачи. При скорости 80 блистеров в минуту и формате блистера 4×7 (28 таблеток в блистере) за одну смену продолжительностью 8 часов производится около 1,08 млн таблеток - достаточно для большинства мелкосерийных контрактов CMO. Полуавтоматические машины (15-40 блистеров в минуту) подходят только для производства на стадии НИОКР или клинических испытаний до 50 000 таблеток в день. Машины производительностью более 200 блистеров/мин требуют затрат на валидацию на уровне предприятия, что редко обеспечивает окупаемость инвестиций для CMO производительностью менее 5 млн таблеток в день.
Сколько стоит машина для упаковки блистеров в соответствии с требованиями cGMP для небольшой фармацевтической компании в 2025 году?
Автоматическая машина для блистерной упаковки, соответствующая требованиям cGMP, с документацией IQ/OQ/PQ для малых фармацевтических предприятий стоит от $28 000 до $90 000 долларов США в 2025 году, в зависимости от скорости производства, платформы пленки и пакета документации. Полуавтоматические установки начинаются от $8 000, но обычно не могут генерировать аудиторские записи, необходимые для проверки FDA или EU GMP. Модели для холодной формовки алюмоолова стоят от $55 000 до $150 000+ долларов США. Скрытый фактор стоимости: бюджетные машины по цене $6,000-$18,000 часто требуют $20,000-$50,000 в сторонней валидации для создания документации IQ/OQ/PQ, что полностью исключает кажущееся преимущество цены. Общая стоимость владения оборудованием в течение 5 лет является более точным финансовым показателем, чем только цена покупки. Обратитесь в HIJ, чтобы получить анализ совокупной стоимости владения для конкретного проекта.
Нужна ли мне машина для блистеров из алюминиума или стандартная машина для блистеров из ПВХ для контрактной упаковки фармацевтических препаратов?
Вам нужна машина для холодной формовки блистеров из алюмокалиевого сплава, если какой-либо из API-продуктов вашего клиента гигроскопичен, чувствителен к влаге или требует скорости передачи паров влаги (MVTR) менее 0,1 г/м²-день - требование, которому не может соответствовать стандартная термоформовка ПВХ. MVTR пленки ПВХ обычно составляет 1,5-3,0 г/м²-день; ПВХ с PVDC-покрытием улучшает этот показатель до 0,3-0,5 г/м²-день; алюмоалю в холодной форме достигает <0,01 г/м²-день. API, включая ингибиторы протонного насоса, шипучие таблетки, сублингвальные пленки и многие онкологические препараты, требуют барьерной защиты alu-alu. Для CMO, создающего универсальный портфель, стратегическими инвестициями являются одна линия alu-alu и одна линия термоформования, покрывающие 95%+ регулируемого рынка фармацевтической упаковки. Если бюджет ограничивает вас одной платформой, термоформовочная машина с возможностью использования пленки PVDC обслуживает большую часть объема CMO.
Каков самый быстрый способ провалить аудит FDA или GMP ЕС, связанный с блистерной упаковкой?
Три самых быстрых способа получить критическое заключение по GMP, связанное с блистерной упаковкой, это: (1) работа без заполненной документации IQ на установленное оборудование, (2) внесение изменений в поставщика формовочной пленки или спецификацию пленки для укупорки без записи о контроле изменений и (3) наличие записей партии ПЛК, изменяемых вручную без аудиторского контроля - прямое нарушение 21 CFR Part 11. По моему опыту проведения более 40 аудитов на предприятиях в Юго-Восточной Азии и Латинской Америке, отсутствие документации IQ является наиболее распространенной проблемой, связанной с блистерной линией, - на нее указывают примерно 65% замечаний FDA 483, связанных с упаковкой, на предприятиях с числом сотрудников менее 50 человек. Согласно Разделу 8.3 Приложения 1 к GMP ЕС (пересмотр 2022 года), записи о целостности уплотнений должны вестись для каждой партии; отсутствие автоматизированной регистрации данных является критическим (Grade 1) результатом инспекций MHRA ЕС.
Как оценить китайского производителя блистерных упаковочных машин для контрактной поставки фармацевтической продукции?
Оценивайте китайского производителя блистерных упаковочных машин по пяти проверяемым критериям, а не по маркетинговым заявлениям: Сертификат CE с номером нотифицированного органа, образец пакета шаблонов IQ/OQ/PQ, список клиентов на регулируемых рынках (FDA/EU), возможность проведения аудита на заводе и письменная гарантия наличия запасных частей в течение минимум 10 лет.
- Сертификат CE: Требуйте декларацию соответствия CE, подписанную уполномоченным лицом, со ссылкой на конкретные директивы (Директива по машинному оборудованию 2006/42/EC; Директива по электромагнитной совместимости). Знак CE на заводской табличке машины без подтверждающих документов не является действительным доказательством.
- Шаблоны IQ/OQ/PQ: Запросите фактический шаблон, а не заявление о том, что шаблоны существуют. Оцените, есть ли в них прямая ссылка на применимые требования EU GMP Annex 15 и 21 CFR Part 211.
- Ссылки: Обратитесь как минимум к двум представителям компании и спросите: Выполняла ли машина заявленные характеристики во время FAT? Были ли документы IQ/OQ/PQ пригодны для использования без существенного пересмотра? Как поставщик реагировал на дефекты первого года эксплуатации?
- Заводской аудит: Любой производитель, не желающий проводить аудит (лично или по видеосвязи), должен быть исключен из вашего списка, независимо от цены.
- Запасные части: Определите 8-12 наиболее изнашиваемых компонентов и уточните региональные складские запасы и время выполнения заказа для каждого из них. Срок изготовления уплотнительного штампа составляет 16 недель, что означает 16-недельную остановку производства для каждой замены.
HIJ Machinery ведет публичный Почему HIJ Страница с подробным описанием наших сертификатов качества, поддержки валидации и глобального портфеля эталонных проектов.
Сколько времени занимает валидация IQ/OQ/PQ для линии блистерной упаковки в небольшой компании CMO?
Полная валидация IQ/OQ/PQ для машины для блистерной упаковки в небольшой CMO обычно занимает 8-14 недель с момента поставки машины до утверждения отчета PQ - при условии, что инженерные сети на объекте готовы, шаблоны IQ/OQ предварительно одобрены отделом контроля качества, а во время выполнения OQ не возникает критических отклонений. Наиболее распространенные факторы, нарушающие сроки: (1) задержки с готовностью оборудования - 3-6 недель можно избежать с помощью контрольного списка перед установкой; (2) циклы пересмотра шаблонов IQ - 2-4 недели, если шаблоны нужно переписывать с нуля (это не проблема с шаблонами, поставляемыми HIJ); (3) отклонения OQ, требующие CAPA перед PQ - добавляется 2-6 недель на каждое отклонение. Для ОКУ, у которых сроки выполнения контракта поджимают, критическим пунктом пути является утверждение шаблона в отделе контроля качества: начните этот процесс за 6 недель до поставки машины, используя пакет шаблонов HIJ в качестве начального проекта.
Мои блистерные уплотнения не выдерживают испытания на вакуумное разложение - какова наиболее вероятная причина и ее устранение?
Нарушение герметичности блистера при испытании на вакуумное разрушение (USP Method B) чаще всего вызвано тремя основными причинами: смещением температуры запечатывающей губки (>±5°C от установленного значения), смещением твердости запечатывающей прокладки (увеличение на 15+ пунктов по Шору А) или несоответствием натяжения пленки, вызывающим микроморщины в зоне тепловой герметизации.
- 🔴 Температурный дрейф: Повторно откалибруйте термопару уплотнительной губки; проверьте дрейф термопары с помощью эталона, отслеживаемого NIST. Если дрейф подтверждается, замените термопару и откалибруйте ПИД-регулятор. Цель: ≤±2°C равномерность поперечной щеки при подтвержденной уставке (обычно 160-190°C для алюминиевых крышек на ПВХ).
- 🔴 Твердость прокладки: Проверьте твердость уплотнительной прокладки с помощью дюрометра по Шору A. Если показания превышают исходную спецификацию на >10 пунктов по Шору А, замените прокладку. Стандартный интервал замены: 400-600 часов работы для силиконовых прокладок HTV. Документируйте замену как событие ТО в журнале учета оборудования.
- 🔴 Натяжение фольги: Измерьте натяжение фольги с помощью тензодатчика на станции размотки; цель - 2,0-3,0 Н ± 0,3 Н. Отрегулируйте натяжение тормоза или установите сервоуправление натяжением, если ручная регулировка не может обеспечить ±0,5 Н. После каждой регулировки повторно проведите 30 пробный тест на целостность уплотнения, прежде чем возобновлять промышленное производство.
Готовы выбрать блистерную машину с нулевым риском для соблюдения нормативных требований?
Расскажите нам о своем ассортименте продукции, целевых объемах производства и нормативно-правовом регулировании рынка - команда Forester разработает решение для блистерной упаковки, соответствующее требованиям, которое будет соответствовать вашим контрактам, а не только текущему размеру партии.
“В HIJ Machinery я не просто продаю вам машину, я поставляю уверенность в проекте.” - Лесник Сян, Основатель компании HIJ Machinery


